Patogeneza periimplantitisa – kada, kako i zašto?
Katja Bakšić [1]
izv. prof. dr. sc. Ana Badovinac [2]
[1] dr. med. dent., diplomirala ak. god. 2024./25.
[2] Zavod za parodontologiju, Sveučilište u Zagrebu Stomatološki fakultet
Sažetak
Periimplantitis predstavlja jedan od najvećih izazova suvremene stomatologije zbog sve veće upotrebe dentalnih implantata kao rješenja za nadomještanje izgubljenih zuba. Ova bolest upalnog karaktera zahvaća tkiva oko implantata, dovodeći do progresivnog gubitka potpornog koštanog tkiva, što može rezultirati destabilizacijom i gubitkom implantata. Periimplantitis značajno utječe na kvalitetu života pacijenata i predstavlja izazov za stomatološke stručnjake u pogledu dijagnostike, prevencije i liječenja.
Uzročnici periimplantitisa su prvenstveno bakterijski mikroorganizmi koji stvaraju biofilm na površini implantata. Međutim, razvoj bolesti nije uzrokovan isključivo prisutnošću bakterija, već i složenim interakcijama između patogena i imunološkog sustava domaćina. Osim bakterijske infekcije, značajnu ulogu u nastanku periimplantitisa imaju različiti lokalni i sistemski čimbenici rizika, poput loše oralne higijene, pušenja, metaboličkih bolesti poput dijabetesa, te genetske predispozicije.
Iako su u posljednjih nekoliko godina napravljeni značajni pomaci u razumijevanju periimplantitisa, još uvijek je potrebno provesti dodatna znanstvena istraživanja kako bi se dobila točna, detaljna i jasna slika o mehanizmima nastanka i razvoju bolesti. Takva saznanja omogućila bi razvoj učinkovitijih metoda prevencije i terapije te poboljšala dugoročnu uspješnost dentalnih implantata.
Ključne riječi: periimplantitis; patogeneza; bakterijski biofilm; čimbenici rizika
Uvod
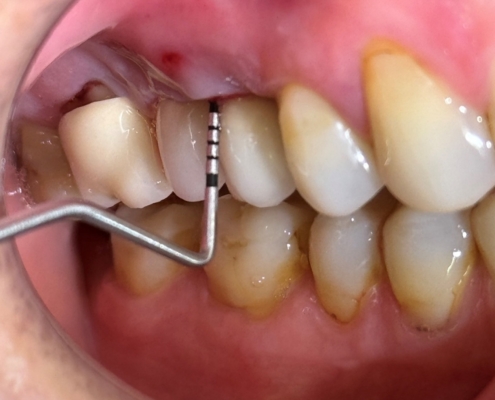
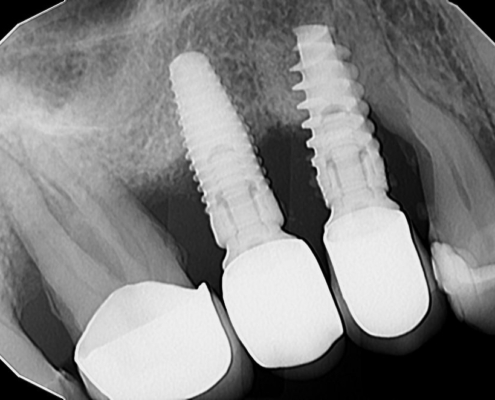
Periimplantitis je upalno patološko stanje koje zahvaća tkiva u neposrednoj okolini dentalnog implantata, pri čemu dolazi do upale periimplantatne sluznice i postupnog gubitka koštanog potpornog tkiva. Kliničke manifestacije periimplantitisa uključuju upalu, krvarenje pri sondiranju, supuraciju, povećanu dubinu sondiranja i gubitak kosti (Slika 1.). Upala mekih tkiva obično se otkriva krvarenjem pri sondiranju, dok se gubitak kosti prepoznaje na radiografskim snimkama kao ˝krater˝ oko implantata uz povećane dubine sondiranja (Slika 2.). Dubina sondiranja može ukazivati na ozbiljnost bolesti i korelira s gubitkom kosti, čija brzina varira među pacijentima (1). Periimplantitis se često razvija kod pacijenata s prethodnom anamnezom uznapredovalog parodontitisa, lošom kontrolom plaka te nedostatkom redovite terapije održavanja nakon implantološkog zahvata.
Faktori rizika
Prije upuštanja u implantoprotetsku terapiju potrebno je ustanoviti, za svakog pacijenta individualno, ima li neke faktore rizika koji bi mogli umanjiti uspješnost terapije. Među sistemskim faktorima rizika najznačajnija je povijest upalne parodontne bolesti – parodontitisa budući da pacijenti s takvom anamnezom imaju dokazano povećan rizik od razvoja periimplantitisa. Pušenje također značajno doprinosi gubitku pričvrstka i gubitku zuba (2). Diabetes mellitus je metabolička bolest koja negativno utječe na imunološki sustav i metabolizam kostiju (3), kao i na sastav mikrobioma, čak i kada su parodontna tkiva zdrava (4). Od lokalnih faktora važnu ulogu u razvoju periimplantitisa imaju loša oralna higijena i neredovita potporna terapija nakon implantacije. Kod takvih pacijenata je dokazan klinički gubitak pričvrstka, što naglašava važnost samostalne i profesionalne kontrole infekcije u sprječavanju parodontnih i periimplantatnih bolesti (5). Manjak keratinizirane sluznice ( <2 mm) može otežati samostalno održavanje oralne higijene, što dovodi do većeg nakupljanja plaka, krvarenja pri sondiranju, upale i povlačenja sluznice (6). Višak cementa može potaknuti upalni odgovor u periimplantnim tkivima, osobito zato što hrapava površina cementa pogoduje nakupljanju biofilma i zadržavanju bakterija (7). Okluzijsko preopterećenje također može pridonijeti gubitku kosti oko implantata, posebice kada je prisutna i bakterijska infekcija. (2).
Uloga bakterijske mikrobiote i biofilma u razvoju periimplantitisa
Zdravi i oboljeli implantati pokazuju značajne razlike u sastavu mikroorganizama (8). Mikrobiota zdravog implantata u većoj količini sadrži gram-pozitivne fakultativne štapiće i koke, sa tek ponekom prisutnom gram-negativnom anaerobnom bakterijskom vrstom. Takav okoliš uspijeva održavati gingivno i periimplantatno zdravlje (9). Kod periimplantitisa, mikrobiota se sastoji od heterogene mješavine u kojoj su smanjeni korisni mikroorganizmi, dok su patogeni prisutni u većoj mjeri, često uključujući bakterije povezane s upalnim procesima parodonta (10). To prvenstveno uključuje gram-negativne i anaerobne bakterijske vrste (11,12). Također, periimplantatni džep karakterizira povećana količina bakterija iz tzv. ˝crvenog kompleksa˝, Porphyromonas gingivalis, Tannerella forsythia i Treponema denticola (13), a dokazana je i povećana učestalost bakterija Aggregatibacter actinomycetemcomitans i Prevotella intermedia (14).
Biofilm također ima ključnu ulogu u nastanku i razvoju periimplantitisa. Proces stvaranja biofilma započinje formiranjem pelikule, koja se sastoji od salivarnih proteina i peptida, na površini implantata. Na nju se, u početku, nakupljalju primarni kolonizatori kao što su Streptococcus sanguinis i bakterije roda Actinomyces. Oni mijenjaju sastav biofilma koji pogoduje naseljavanju sekundarnih kolonizatora. Takva struktura biofilma ne samo da štiti bakterije od obrambenih mehanizama domaćina, već i mijenja uvjete unutar istog, postupno formirajući anaerobnu okolinu (15). Riječ je o kompleksnim bakterijskim zajednicama koje su uložene u matriks, zbog čega je dodatno otežano njihovo uklanjanje. Kada dođe do poremećaja ravnoteže između korisnih i štetnih mikroorganizama u periimplantatnom području, nastaje disbioza – stanje koje potiče razvoj kronične upale. Patogeni mikroorganizmi mogu modulirati imunološke odgovore domaćina, inhibirajući učinkovitu fagocitozu i upalne procese koji bi inače kontrolirali infekciju. Disbioza potiče i proizvodnju upalnih citokina poput IL-1β i TNF-α koji dodatno pogoršavaju tkivnu destrukciju (16). Zbog ograničenih regenerativnih sposobnosti periimplantatnih tkiva, obrambeni mehanizmi domaćina često nisu dovoljni za zaustavljanje infekcije.
Upalni odgovori i imunološki mehanizmi
Gubitak kosti oko već integriranog dentalnog implantata nastaje kao posljedica širenja upalnog infiltrata u okolno vezivno tkivo, pri čemu ključnu ulogu imaju osteoklasti – multinuklearne stanice odgovorne za razgradnju koštanog tkiva. U zdravim fiziološkim uvjetima, njihova aktivnost je uravnotežena s djelovanjem osteoblasta, koji izgrađuju kost. Međutim, u prisutnosti upale ta se ravnoteža narušava (17). U periimplantitisu, upalne stanice izlučuju signalne molekule, poput interleukina, prostaglandina i tumorskog faktora nekroze (TNF-α), koje potiču diferencijaciju i aktivaciju osteoklasta. Shodno tome, povećana aktivnost osteoklasta uzrokuje resorpciju kosti, što se smatra mehanizmom obrane kojim se tijelo pokušava udaljiti od izvora upale (17).
Imunološki odgovor kod periimplantitisa nastaje kao rezultat međudjelovanja urođene i stečene imunosti. Urođena imunost djeluje kao prva linija obrane, pružajući brzu, nespecifičnu reakciju kroz upalne medijatore i sustav komplementa radi početnog ograničavanja infekcije (16). Ovaj obrambeni mehanizam se aktivira prepoznavanjem različitih uzročnika bolesti, uključujući bakterije i viruse, upalne citokine (TNF i interferoni) te molekule koje signaliziraju oštećenje stanica, nakon čega stečena imunost pruža ciljani odgovor putem T i B limfocita, omogućujući učinkovitije uklanjanje mikroorganizama te formiranje imunološke memorije (18).
Makrofagi, ključne stanice urođene imunosti, imaju značajnu ulogu u regulaciji koštane ravnoteže i procesu oseointegracije dentalnih implantata (19). Istraživanja su pokazala da se ove stanice brzo nakupljaju na površinama implantata prije početka formiranja kosti, čime pozitivno doprinose stvaranju i mineralizaciji novog koštanog tkiva (20,21). Jedna od najbitnijih karakteristika je njihova sposobnost prilagodbe ili plastičnost, što im omogućuje preuzimanje različitih funkcionalnih fenotipa. Tako makrofagi mogu poprimiti M1 fenotip (pro-upalni, uključen u imunološku obranu) ili M2 fenotip (antiupalni, usmjeren na regeneraciju tkiva) (22). Ova M1/M2 os odražava suprotne aktivnosti makrofaga: dok M1 fenotip inhibira proliferaciju stanica i uzrokuje oštećenje tkiva, M2 fenotip potiče obnovu stanica i regeneraciju oštećenih struktura (23). Makrofagi se mogu polarizirati kao odgovor na različite podražaje, kao što je npr. bakterijska infekcija, nakon čega izlučuju brojne pro-upalne citokine, koji ne samo da stvaraju snažan upalni odgovor već i privlače dodatne imunološke stanice, pogoršavajući oštećenje tkiva (24). M1 makrofagi su posebno važni u procesu stvaranja osteoklasta jer luče RANKL, protein ključan za metabolizam koštanog tkiva, koji potiče njihovu diferencijaciju i resorpciju kosti (25). Nadalje, oni proizvode reaktivne kisikove spojeve (ROS) i enzime poput matriksnih metaloproteinaza (MMP), koji dodatno razgrađuju koštano tkivo (26). Osim u bakterijski induciranim upalnim procesima, makrofagi sudjeluju i u aseptičnim upalama koje nastaju kao odgovor na otpuštanje titanskih čestica s površine dentalnih implantata (16).
Neutrofili također sudjeluju u imunološkom odgovoru domaćina. Njihova količina na mjestu infekcije mora biti pažljivo uravnotežena – dovoljno visoka za učinkovito uklanjanje patogena, ali ne i pretjerana, kako bi se izbjegle štetne posljedice po vlastito tkivo i razvoj imunopatoloških reakcija (27). Nakon aktivacije, neutrofili provode fagocitozu, formiraju fagolizosome te oslobađaju ROS i proteolitičke enzime za uništavanje mikroorganizama. Uz svoju primarnu funkciju u imunološkoj obrani i regulaciji, oni također komuniciraju s osteocitima te utječu na upalne procese resorpcije kosti (28).
Dendritičke stanice ključne su višefunkcionalne stanice koje povezuju prirođeni i stečeni imunosni sustav. Imaju sposobnost prepoznavanja antigena te njihova prezentiranja T limfocitima, čime pokreću niz upalnih odgovora (29). No, pretjerana aktivacija stečenog imunološkog odgovora može izazvati oštećenja okolnih tkiva, što dodatno otežava kliničku sliku periimplantitisa.
Nakon prepoznavanja antigena od strane antigen-prezentirajućih stanica, T limfociti postaju aktivni, prvenstveno se diferenciraju u CD4+ i CD8+ T stanice, te oblikuju imunološki mikrookoliš oko implantata. Kod periimplantitisa, aktivirane CD4+ T stanice dominiraju upalnim infiltratom. One luče povećanu količinu upalnih medijatora koji potiču diferencijaciju osteoklasta, čime se ubrzava razgradnja kosti i pogoršava tijek bolesti (25,30). Osim T limfocita, i B limfociti imaju važnu ulogu – diferenciraju se u plazma stanice koje proizvode specifična antitijela, čime doprinose neutralizaciji patogena. U lezijama periimplantitisa značajno je povišena razina B limfocita, uz istodobno povećane koncentracije IL-1β, TNF-α, IL-4 i osnovnog fibroblastnog faktora rasta (31). Ipak, s obzirom na specifičnu anatomiju periimplantatnog područja, koje oskudijeva mekim tkivima i tjelesnim tekućinama, smatra se da B limfociti imaju samo pomoćnu ulogu u periimplantitisu, prvenstveno kroz regrutaciju drugih imunoloških stanica (32). Međutim, prekomjerna ili poremećena imunološka aktivacija, posebno ako je dugotrajna, može uzrokovati razgradnju alveolarne kosti i oštećenje mekih tkiva, što dodatno komplicira liječenje periimplantitisa (31).
Utjecaj genetike i okolišnih čimbenika
Iako se periimplantitis primarno povezuje s mikrobiološkim i mehaničkim čimbenicima, sve više dokaza upućuje na važnu ulogu genetske predispozicije u njegovom razvoju. Određene varijacije u genima, poznate kao genetski polimorfizmi, mogu utjecati na izraženost upalnih procesa i sposobnost organizma da se nosi s bakterijskim izazovima u periimplantatnim tkivima. Posebno su istaknuti polimorfizmi u genima za interleukine, TNF-α, metaloproteinaze matriksa i faktore rasta uključene u metabolizam kosti koji mogu narušiti ravnotežu između upalnih i regenerativnih procesa (33). Takve genetske varijacije povezane su s pojačanim lučenjem upalnih medijatora te aktivacijom stanica koje sudjeluju u razgradnji koštanog tkiva, čime se povećava rizik od gubitka kosti i dugoročnog neuspjeha implantata. Osim toga, dokazano je da tkiva zahvaćena periimplantitisom pokazuju promjene u staničnom sastavu – prisutnost fibro-osteoblastičnih stanica koje imaju slabiju sposobnost formiranja kosti, što dodatno otežava regeneraciju (34, 35). Pušenje, kao i ostali čimbenici rizika, može pojačati učinak genetske predispozicije te dodatno narušiti sposobnost organizma da kontrolira upalne procese. Ono mijenja subgingivni bakterijski profil tako što smanjuje broj korisnih komenzalnih, a povećava prisutnost patogenih bakterija. Osim toga, pušenje nepovoljno utječe na cijeljenje rana te uzrokuje smanjenu gustoću kosti oko implantata i slabiji kontakt između kosti i implantata, što povećava rizik od periimplantitisa. Kod pušača su izmjerene povišene razine upalnih citokina, dublji parodontni džepovi te veća prisutnost upalnih bakterija u periimplantatnom tkivu u usporedbi s nepušačima. Istraživanja također potvrđuju da je u mikrobiološkom sastavu pušača prisutna disbioza, neovisno o njihovu parodontnom statusu (36).
Uloga titanskih čestica u razvoju periimplantitisa
Titan i njegove legure često se koriste u dentalnoj implantologiji zbog svoje otpornosti na koroziju, biokompatibilnosti i mehaničke izdržljivosti (37). Međutim, novija istraživanja ukazuju na to da oslobođene titanske čestice mogu doprinijeti razvoju periimplantitisa putem različitih mehanizama, uključujući reakciju na strano tijelo, stanični odgovor epitelnih, gingivnih, upalnih i koštanih stanica te epigenetske promjene poput metilacije DNA i poticanja disbioze oralnog mikrobioma. Oslobađanje titanskih čestica može se dogoditi u bilo kojoj fazi implantološke rehabilitacije — kirurškoj, protetskoj ili fazi održavanja, a dodatno se može potaknuti i instrumentacijom površine implantata zbog njegove slabe otpornosti na trošenje. Tako tijekom postavljanja implantata dolazi do oštećenja zaštitnog sloja titanijevog oksida, što rezultira otpuštanjem mikroskopskih čestica u okolna tkiva. To izaziva lokalnu upalnu reakciju, pojačanu ekspresiju upalnih citokina poput RANKL, IL-33 i TGF-β1 te narušava stabilnost implantata (38). U okviru koncepta reakcije na strano tijelo smatra se da titanske čestice mogu aktivirati imunološki odgovor te narušiti ravnotežu između osteoblasta i osteoklasta, što u konačnici dovodi do gubitka kosti i progresije periimplantatnih lezija. Istraživanja na ljudskim biopsijama periimplantatnih tkiva dodatno su potvrdila prisutnost titanskih čestica u upalnom infiltratu uz lezije periimplantitisa, s većim koncentracijama iona u odnosu na zdrava periimplantatna mjesta. Provedene su i svjetlosno-mikroskopske analize periimplantatnih tkiva kojima se potvrdila prisutnost titanskih čestica u gotovo 90% uzoraka, često u kombinaciji s kroničnim upalnim infiltratom, a uočeno je i da one manje od 10 μm mogu biti citotoksične te izazvati resorpciju kosti (39). Prema in vivo analizama, titanske čestice smanjuju vijabilnost stanica i s vremenom povećavaju stvaranje reaktivnih kisikovih spojeva (ROS), što dovodi do oksidativnog stresa, povišenih razina titana, poremećene pregradnje kosti i razgradnje kolagena. Posljedično se narušava regrutacija neutrofila, dolazi do disregulacije mezenhimalnih matičnih stanica (MSC) i oslabljene regeneracije kosti (27). Također, iako biokompatibilni, titanijevi implantati tijekom i nakon ugradnje mogu biti podložni biotribokoroziji – oštećenjima uzrokovanima trenjem, korozijom i mikrobiološkim utjecajima, što dovodi do dodatnog oslobađanja titanijevih iona u okolna tkiva. Oni potiču imunološki odgovor organizma koji uključuje aktivaciju makrofaga, uz povećanu proizvodnju upalnih molekula poput IL-1β, IL-8 i IL-18. Takvo upalno stanje narušava proces oseointegracije i potiče širenje patogenih bakterija, čime se periimplantitis dodatno intenzivira (16).
Zaključak
Implantoprotetska terapija zauzima važno mjesto u suvremenoj stomatologiji kao učinkovito rješenje za nadoknadu izgubljenih zuba. Međutim, dentalni implantati mogu biti zahvaćeni stanjima kao što su periimplantatni mukozitis i periimplantitis, gdje je rizik od gubitka implantata vrlo visok. Takve ishode želimo spriječiti, zbog čega se intenzivno fokusiramo na nove spoznaje o patogenezi periimplantitisa, ali i na njegovu prevenciju i terapiju.
Jedan od najvažnijih aspekata u pristupu ovom kliničkom problemu je prevencija, koja se temelji na pravilnom planiranju implantološke terapije, redovitoj kontroli, održavanju oralne higijene te edukaciji pacijenata.
S obzirom na navedeno, razvoj periimplantitisa rezultat je kompleksne interakcije između genetske predispozicije, imunološke disregulacije, mikrobiološke disbioze i utjecaja okolišnih čimbenika poput titanskih čestica i pušenja. Genetski polimorfizmi i poremećaji imunološke ravnoteže značajno doprinose intenzitetu upalnih procesa i gubitku koštane potpore implantata. Nadalje, povećana količina patogenih mikroorganizama remeti homeostazu periimplantatnih tkiva, potičući kroničnu upalu. Ključnu ulogu u patogenezi bolesti igra i imunološki odgovor domaćina, naročito dominacija pro-upalnog fenotipa makrofaga, te posljedično oslobađanje upalnih citokina. Iako titanske čestice pridonose lokalnoj upalnoj reakciji i destabilizaciji implantata, daljnja istraživanja potrebna su za potpunije razumijevanje ovih procesa. Takva saznanja omogućit će razvoj preciznijih dijagnostičkih alata i učinkovitijih terapijskih i preventivnih strategija, s ciljem očuvanja dugoročne funkcionalnosti i stabilnosti dentalnih implantata.
Literatura
- Heitz-Mayfield LJA. Peri-implant mucositis and peri-implantitis: key features and differences. Br Dent J. 2024;236(10):791–4.
- Schwarz F, Derks J, Monje A, Wang HL. Peri-implantitis. J Periodontol. 2018;89(S1):S267–90.
- Pasquel FJ, Lansang MC, Dhatariya K, Umpierrez GE. Management of diabetes and hyperglycaemia in the hospital. Lancet Diabetes Endocrinol. 2021;9(3):174–88.
- Silva DN de A, Casarin M, Monajemzadeh S, Bezerra B de B, Lux R, Pirih FQ. The Microbiome in Periodontitis and Diabetes. Front Oral Health. 2022;3:859209.
- Axelsson P, Lindhe J. The significance of maintenance care in the treatment of periodontal disease. J Clin Periodontol. 1981;8(4):281–94.
- Gobbato L, Avila-Ortiz G, Sohrabi K, Wang CW, Karimbux N. The effect of keratinized mucosa width on peri-implant health: a systematic review. Int J Oral Maxillofac Implants. 2013;28(6):1536–45.
- Staubli N, Walter C, Schmidt JC, Weiger R, Zitzmann NU. Excess cement and the risk of peri-implant disease – a systematic review. Clin Oral Implants Res. 2017;28(10):1278–90.
- Shibli JA, Melo L, Ferrari DS, Figueiredo LC, Faveri M, Feres M. Composition of supra- and subgingival biofilm of subjects with healthy and diseased implants. Clin Oral Implants Res. 2008;19(10):975–82.
- Mombelli A, Décaillet F. The characteristics of biofilms in peri-implant disease. J Clin Periodontol. 2011;38 Suppl 11:203–13.
- Sanz-Martin I, Doolittle-Hall J, Teles RP, Patel M, Belibasakis GN, Hämmerle CHF, et al. Exploring the microbiome of healthy and diseased peri-implant sites using Illumina sequencing. J Clin Periodontol. 2017;44(12):1274–84.
- Belibasakis GN. Microbiological and immuno-pathological aspects of peri-implant diseases. Arch Oral Biol. 2014;59(1):66–72.
- Jansson L, Lundmark A, Modin C, Abadji D, Yucel-Lindberg T. Intra-individual cytokine profile in peri-implantitis and periodontitis: A cross-sectional study. Clin Oral Implants Res. 2021;32(5):559–68.
- Botero JE, González AM, Mercado RA, Olave G, Contreras A. Subgingival microbiota in peri-implant mucosa lesions and adjacent teeth in partially edentulous patients. J Periodontol. 2005;76(9):1490–5.
- Sahrmann P, Gilli F, Wiedemeier DB, Attin T, Schmidlin PR, Karygianni L. The Microbiome of Peri-Implantitis: A Systematic Review and Meta-Analysis. Microorganisms. 2020;8(5):661.
- Leonhardt A, Olsson J, Dahlén G. Bacterial colonization on titanium, hydroxyapatite, and amalgam surfaces in vivo. J Dent Res. 1995;74(9):1607–12.
- Huang M, Wang C, Li P, Lu H, Li A, Xu S. Role of immune dysregulation in peri-implantitis. Front Immunol. 2024;15:1466417.
- Lindhe J, Karring T, Lang NP, editors. Clinical periodontology and implant dentistry. 4th ed. Oxford, UK ; Malden, MA: Blackwell; 2003. 1044 p.
- Zhang Q, Cao X. Epigenetic Remodeling in Innate Immunity and Inflammation. Annu Rev Immunol. 2021;39:279–311.
- Miron RJ, Bosshardt DD. OsteoMacs: Key players around bone biomaterials. Biomaterials. 2016;82:1–19.
- Wang X, Li Y, Feng Y, Cheng H, Li D. The role of macrophages in osseointegration of dental implants: An experimental study in vivo. J Biomed Mater Res A. 2020;108(11):2206–16.
- Chehroudi B, Ghrebi S, Murakami H, Waterfield JD, Owen G, Brunette DM. Bone formation on rough, but not polished, subcutaneously implanted Ti surfaces is preceded by macrophage accumulation. J Biomed Mater Res A. 2010;93(2):724–37.
- Liu YC, Zou XB, Chai YF, Yao YM. Macrophage polarization in inflammatory diseases. Int J Biol Sci. 2014;10(5):520–9.
- M1 and M2 Macrophages: Oracles of Health and Disease – PubMed [Internet]. [cited 2025 May 19]. Available from: https://pubmed.ncbi.nlm.nih.gov/23428224/
- Peng S, Fu H, Li R, Li H, Wang S, Li B, et al. A new direction in periodontitis treatment: biomaterial-mediated macrophage immunotherapy. J Nanobiotechnology. 2024;22:359.
- Li Y, Li X, Guo D, Meng L, Feng X, Zhang Y, et al. Immune dysregulation and macrophage polarization in peri-implantitis. Front Bioeng Biotechnol. 2024;12:1291880.
- Önder YB, Alpaslan NZ. Peri-implant phenotype, calprotectin and MMP-8 levels in cases diagnosed with peri-implant disease. Clin Oral Investig. 2024;28(7):404.
- Bressan E, Ferroni L, Gardin C, Bellin G, Sbricoli L, Sivolella S, et al. Metal Nanoparticles Released from Dental Implant Surfaces: Potential Contribution to Chronic Inflammation and Peri-Implant Bone Loss. Mater Basel Switz. 2019;12(12):2036.
- Chapple ILC, Hirschfeld J, Kantarci A, Wilensky A, Shapira L. The role of the host-Neutrophil biology. Periodontol 2000. 2023;28–9.
- Yin X, Chen S, Eisenbarth SC. Dendritic Cell Regulation of T Helper Cells. Annu Rev Immunol. 2021;39:759–90.
- Bertoldo BB, Paulo GO, Furtado TC de S, Pereira TL, Rodrigues Junior V, Rodrigues DBR, et al. New immunological aspects of peri-implantitis. Einstein Sao Paulo Braz. 2024;22:eAO0396.
- Malmqvist S, Clark R, Johannsen G, Johannsen A, Boström EA, Lira-Junior R. Immune cell composition and inflammatory profile of human peri-implantitis and periodontitis lesions. Clin Exp Immunol. 2024;217(2):173–82.
- Wang CW, Hao Y, Di Gianfilippo R, Sugai J, Li J, Gong W, et al. Machine learning-assisted immune profiling stratifies peri-implantitis patients with unique microbial colonization and clinical outcomes. Theranostics. 2021;11(14):6703–16.
- Chen X, Zhao Y. Genetic Involvement in Dental Implant Failure: Association With Polymorphisms of Genes Modulating Inflammatory Responses and Bone Metabolism. J Oral Implantol. 2019;45(4):318–26.
- Schminke B, Vom Orde F, Gruber R, Schliephake H, Bürgers R, Miosge N. The Pathology of Bone Tissue during Peri-Implantitis. J Dent Res. 2015 Feb;94(2):354–61.
- Jacobi-Gresser E, Huesker K, Schütt S. Genetic and immunological markers predict titanium implant failure: a retrospective study. Int J Oral Maxillofac Surg. 2013;42(4):537–43.
- Chih SM, Cheng CD, Chen SH, Sung CE, Huang RY, Cheng WC. The impact of smoking on peri-implant microbiota: A systematic review. J Dent. 2023;133:104525.
- Xie Y, Li S, Zhang T, Wang C, Cai X. Titanium mesh for bone augmentation in oral implantology: current application and progress. Int J Oral Sci. 2020;12(1):37.
- Chen L, Tong Z, Luo H, Qu Y, Gu X, Si M. Titanium particles in peri-implantitis: distribution, pathogenesis and prospects. Int J Oral Sci. 2023;15(1):49.
- Asa’ad F, Thomsen P, Kunrath MF. The Role of Titanium Particles and Ions in the Pathogenesis of Peri-Implantitis. J Bone Metab. 2022;29(3):145–54.