Što trebamo znati o farmakologiji Botulinum toksina?
Karla Poljančić [1]
Izv. prof. dr. sc, Ivana Šutej [2]
[1] Studentica šeste godine, Stomatološki fakultet Sveučilišta u Zagrebu
[2] Katedra za farmakologiju, Sveučilište u Zagrebu Stomatološki fakultet
Sažetak
Članak pruža sveobuhvatan pregled temeljne farmakologije botulinum toksina (BoNT), obuhvaćajući uz to i njegovu povijest od smrtonosnog otrova do ključnog lijeka u neurologiji i estetskoj medicini. Detaljno je opisan molekularni mehanizam djelovanja, gdje toksin privremeno prekida komunikaciju između živca i mišića cijepanjem SNARE proteina, čime se blokira oslobađanje neurotransmitera acetilkolina. Opisane su razlike sedam serotipova botulinum toksina. U kliničkoj praksi dominira serotip BoNT-A zbog svoje duge učinkovitosti, primjenjuje se za indikacije kao što su bruksizam, kronične migrene i estetske korekcije bora. BoNT posjeduje i značajan analgetski učinak, koji se objašnjava smanjenjem otpuštanja neuropeptida boli iz nociceptivnih vlakana. Također, opisan je i učinak BoNT na mišiće i žlijezde slinovnice. Unatoč privremenom i reverzibilnom djelovanju, nuspojave poput lokalne slabosti mišića ili asimetrije lica nisu zanemarive te su opisane. Nuspojave najčešće nastaju zbog nekontrolirane difuzije toksina, zbog čega je precizna aplikacija ključna.
Ključne riječi po MeSH-u:
- Botulinum Toxin
- Botulinum Neurotoxin A
- SNARE Proteins
- Neuromuscular junction
Uvod
Malo koja tvar u medicini ima povijest toliko paradoksalnu kao botulinum toksin. Od smrtonosnog „kobasičnog otrova“ do jednog od najvažnijih lijekova u neurologiji i estetici, njegov je put trajao više od 200 godina i temelji se na zanimljivom paradoksu da je najotrovnija supstanca poznata čovjeku postala vrijedan terapijski alat, isključivo ovisno o dozi. Od prvih opisa smrtonosnih trovanja hranom u 19. stoljeću do suvremenih nekirurških tehnika pomlađivanja i liječenja orofacijalnih poremećaja, botulinum toksin prošao je iznimno transformativan razvoj. Danas zauzima važno mjesto u neurologiji, dermatologiji i sve više u dentalnoj medicini. Kako bi se razumjela njegova široka primjena i sigurnosni profil, ključno je poznavati njegovu strukturu, mehanizam djelovanja, razlike među serotipovima te kliničke učinke koji proizlaze iz privremene neuromuskularne blokade.
Povijest
Priča o botulinum toksinu započinje početkom 19. stoljeća u jugozapadnoj Njemačkoj, gdje su se nakon Napoleonovih ratova počeli pojavljivati misteriozni i često smrtonosni slučajevi paralize uzrokovani trovanjem hranom. Njemački doktor i pjesnik, dr. Justus Kerner, primijetio je da je vjerojatno krivac nepoznata tvar koja se nalazila u kobasicama. Već tada je Kerner zaključio kako bi se ta tvar mogla jednog dana koristiti u terapijske svrhe. Krajem 19. stoljeća belgijski mikrobiolog Emile Pierre van Ermengem otkrio je bakteriju odgovornu za trovanje i nazvao je Bacillus botulinus (danas Clostridium botulinum), po latinskoj riječi botulus, odnosno kobasica. A neurotoksin koji ta bakterija proizvodi nazvan je botulinum toksin. Tijekom 20. stoljeća identificirano je više tipova toksina (A–G), a učestalija upotreba konzervirane hrane dodatno je povećala broj slučajeva botulizma. Za vrijeme Drugog svjetskog rata botulinum toksin bio je proučavan i u kontekstu biološkog oružja, a tek 60-ih i 70-ih godina prošlog stoljeća dr. Alan Scott započinje istraživanje njegove primjene u terapijske svrhe kao nekirurška terapija liječenja strabizma. 1989. godine FDA odobrava korištenje botulinum toksina A (BoNT-A) za liječenje strabizma i blefarospazma. Ubrzo nakon toga događa se slučajan, ali povijesan trenutak: oftalmologinja dr. Jean Carruthers primijetila je da pacijentima kojima je liječila blefarospazam nestaju i bore mrštilice. To je bio početak potpuno nove ere u estetskoj medicini. Tijekom 90-ih interes za botoks je eksplodirao, a 2002. FDA odobrava primjenu za estetsko smanjenje glabellarnih bora. Uslijedila su odobrenja za brojne terapijske indikacije (neuralgije, hiperhidroza, hipersalivacija, bruksizam, problemi s TMZ-om, migrene…), a botoks je postao jedan od najistraživanijih i najraširenijih neuromodulatora u medicini i stomatologiji. (1)
Serotipovi i primjena
Botulinum toksin se u prirodi pojavljuje u sedam glavnih serotipova: A, B, C, D, E, F i G. U humanoj medicini primjenu su pronašla ponajprije dva, serotip A i serotip B, dok se ostali uglavnom koriste u svrhe istraživanja. (2)
Serotip A (BoNT-A) najzastupljeniji je u kliničkoj praksi, ponajprije zbog dugog trajanja učinka i stabilnog sigurnosnog profila. Njegova je primjena iznimno široka: od liječenja distonija, spasticiteta, kronične migrene i hiperhidroze do kontrole sialoreje i brojnih estetskih indikacija poput korekcije dinamičkih bora, hipertrofije masetera, gummy smilea ili asimetričnog osmijeha. U stomatološkoj medicini BoNT-A zauzima sve važnije mjesto, osobito u terapiji bruksizma, temporomandibularnih poremećaja, trigeminalne neuralgije, orofacijalnih distonija i sialoreje. Njegovu učinkovitost i sigurnost potvrđuju brojna randomizirana klinička istraživanja. (3–10)
Serotip B (BoNT-B) rjeđe se primjenjuje, najčešće kod pacijenata koji razviju rezistenciju na BoNT-A ili kod određenih autonomnih indikacija poput sialoreje i izrazite hiperhidroze. Međutim, njegov učinak kraće traje, a učestalost nuspojava viša je, što ograničava njegovu rutinsku primjenu. (11–12)
Trajanje djelovanja botulinum toksina ovisi o serotipu, primijenjenoj dozi, anatomskom području te individualnim karakteristikama pacijenta. U estetskim i stomatološkim indikacijama BoNT-A najčešće djeluje 3 do 5 mjeseci, dok BoNT-B traje 2 do 3 mjeseca. Ovi vremenski okviri rezultat su reverzibilne blokade SNARE proteina i postupne regeneracije neuromuskularne spojnice, uključujući sintezu novih proteina i aksonalni sprouting. (7, 11, 13)
Na europskom tržištu dostupni su sljedeći komercijalni pripravci:
- OnabotulinumtoxinA (Botox®)
- AbobotulinumtoxinA (Dysport®)
- IncobotulinumtoxinA (Xeomin®)
- LetibotulinumtoxinA (Letybo®)
- RimabotulinumtoxinB (NeuroBloc®/Myobloc®)
Svi navedeni pripravci odobreni su za različite medicinske i estetske indikacije od strane Europske agencije za lijekove (EMA), a pojedini i od strane FDA. Razlikuju se u pogledu sastava, prisutnosti kompleksirajućih proteina, difuzije i imunogenosti, što može značajno utjecati na klinički odgovor te potencijal za nuspojave. (10-12)
Mehanizam djelovanja
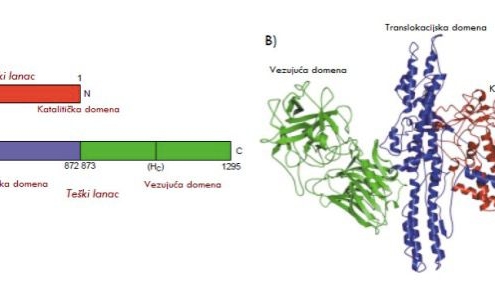
Kako bi se razumjele razlike među pripravcima i način na koji utječu na terapijski učinak, važno je poznavati i molekularni mehanizam djelovanja botulinum toksina. Botulinum toksin djeluje poput visoko specijaliziranog „prekidača“ koji privremeno utiša komunikaciju između živca i mišića. Molekula toksina teška je oko 150 kDa i sastoji se od jednog lanca koji se nakon aktivacije cijepa na teški (100 kDa) i laki lanac (50 kDa), povezane disulfidnom vezom. Teški lanac možemo zamisliti kao “adresu i ključ”, a laki lanac kao “škare” koje obavljaju stvarni posao unutar živčane stanice (14-17). (Slika 1)
Teški lanac ima dvije funkcionalne domene: jedna prepoznaje specifične receptore na površini neurona (gangliozide i proteinske receptore poput SV2 ili synaptotagmina), a druga omogućuje da se laki lanac prevede iz endosoma u citosol živca (14-17).
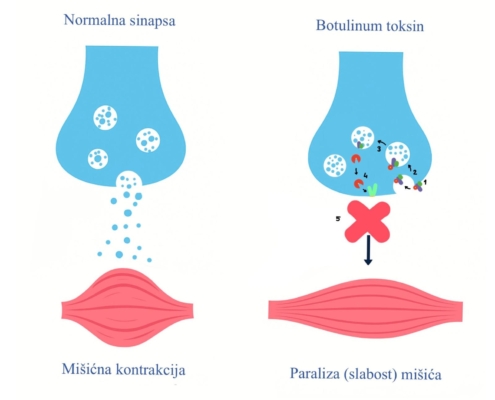
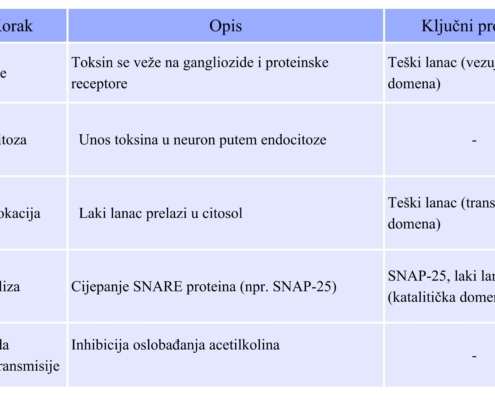
Kad jednom uđe u citosol, laki lanac, cink-ovisna endopeptidaza, precizno cijepa SNARE proteine koji živcu omogućuju da se vezikula s acetilkolinom spoji na membranu i ispusti neurotransmiter (14-17). Tri glavna SNARE proteina su synaptobrevin (VAMP), syntaxin i SNAP-25. Različiti serotipovi botulinum toksina ciljaju različite od njih što utječe na duljinu djelovanja pripravka: BoNT/A i E SNAP-25, BoNT/B, D, F i G VAMP, a BoNT/C syntaxin i SNAP-25. (14, 17). Cijepanjem tih proteina živac više ne može otpustiti acetilkolin, jer je onemogućeno priključivanje vezikula s neurotransmiterima na presinaptičku membranu i posljedično egzocitoza neurotransmitera. Ciljna stanica tako ne dobiva signal, što dovodi do izostanka funkcije. (Slika 2, tablica 1)
Učinak na mišiće
Dolazi do flacidne paralize jer s obzirom da ne dolazi do otpuštanja acetilkolina, nikotinski receptori ostaju neaktivirani te ne dolazi do depolarizacije i stvaranja akcijskog potencijala. (19-20)
Učinak na žlijezde
Isti princip vrijedi i za egzokrine žlijezde. Budući da autonomni živci koji inerviraju slinovnice, znojnice i suzne žlijezde također koriste acetilkolin, botulinum toksin blokira signal i tako smanjuje sekreciju. Taj je učinak lokaliziran na mjestu primjene i reverzibilan, pa se koristi kod hiperhidroze, sialoreje i drugih stanja prekomjernog lučenja (21).
Analgetski učinak
Osim mišićne relaksacije, botulinum toksin ima i analgetski učinak, koji se ne može objasniti samo slabijom napetošću mišića. On smanjuje oslobađanje bolnih neurotransmitera i neuropeptida iz perifernih nociceptivnih vlakana, na primjer glutamata, substance P i CGRP, čime umanjuje neurogenu upalu i osjetljivost nociceptora (24-25).
Toksin također modulira receptore uključene u provođenje boli (TRPV1, NK-1, purinergičke receptore te natrijske i kalcijeve kanale), a putem retrogradnog transporta može utjecati i na centralnu senzibilizaciju, mijenjajući ekspresiju gena u dorzalnim ganglijima i smanjujući aktivaciju mikroglije i pro-nociceptivnih citokina (24, 26-27).
Reverzibilnost
Iako djeluje snažno, učinak botulinum toksina je privremen. Toksin ne uništava živčane završetke; samo privremeno „isključuje“ njihov mehanizam komunikacije. Oporavak se odvija kroz dva procesa:
- živčani završeci stvaraju nove aksonske izdanke (sprouting) koji ponovno uspostavljaju neuromuskularne spojeve,
- živac sintetizira nove, funkcionalne SNARE proteine, čime se vraća normalno oslobađanje acetilkolina i kontraktilnost mišića (22-23).
Nuspojave i neželjene reakcije
Nuspojave botulinum toksina najčešće su posljedica njegove neželjene difuzije u susjedne mišiće. Sistemske nuspojave iznimno su rijetke, a imunološka rezistencija javlja se tek kod dugotrajne terapije i visokih doza.
Većina reakcija blaga je, prolazna i usko povezana s tehnikom primjene. Najčešće nuspojave povezane s primjenom botulinum toksina u stomatologiji uključuju lokalnu slabost mišića, disfagiju (osobito kod primjene u lingvalnoj i oromandibularnoj regiji), asimetriju lica, privremene poremećaje govora i žvakanja te lokalnu bol, hematom ili otok na mjestu primjene. (9, 28-31) Disfagija je najčešće prijavljena ozbiljna nuspojava kod liječenja oromandibularnih distonija, no najčešće je blaga do umjerena i prolazna. (28) Rjeđe se javljaju suhoća usta, parestezije, lokalizirana atrofija mišića i prolazni poremećaji mimike. (9) Pogrešna aplikacija može zahvatiti susjedne mišiće te dovesti do asimetrije osmijeha ili slabosti lica, osobito u estetskim i funkcionalnim stomatološkim indikacijama. (9)
Dugoročno se razmatra mogućnost smanjenja debljine kortikalne kosti mandibule nakon ponovljenih injekcija u maseter i temporalis, iako su u ljudi te promjene minimalne i rijetko klinički značajne. (32) Sistemske nuspojave izuzetno su rijetke i uključuju alergijske reakcije, glavobolju, umor i simptome nalik gripi. (33) Većina nuspojava blaga je i prolazna te ovisi o dozi, tehnici aplikacije i iskustvu kliničara. (29, 31, 34)
Difuzija toksina je njegovo pasivno širenje izvan ciljane regije. Na difuziju utječu volumen injekcije, koncentracija, veličina i anatomija ciljanog mišića te svojstva same formulacije. (3, 35-36) Veći volumen i niža koncentracija povećavaju mehaničko širenje, dok precizna aplikacija manjeg volumena smanjuje rizik neželjenog zahvaćanja okolnih struktura. (35-36)
U stomatologiji i estetskoj medicini neželjena difuzija može uzrokovati slabost susjednih mišića, asimetriju osmijeha, disfagiju ili poremećaje žvakanja, osobito u perioralnom i periorbitalnom području. (3, 30, 36-37) Različite formulacije BoNT-A pokazuju različite profile difuzije — abobotulinumtoxinA ima šire područje djelovanja od onabotulinumtoxinA i incobotulinumtoxinA, što potvrđuju in silico modeli. (3)
Optimalan terapijski učinak i minimalan rizik nuspojava postižu se pravilnim odabirom preparata, preciznim doziranjem, kontroliranim volumenom (npr. ≤0,045 mL po točki u glabellarnom području) i dobrom poznavanjem anatomije. (35-36)
Zaključak
Botulinum toksin, unatoč svojoj povijesnoj reputaciji smrtonosnog otrova, danas je jedan od najvažnijih i najraznovrsnijih terapeutskih alata u neurologiji, dermatologiji i dentalnoj medicini. Razumijevanje njegove strukture, mehanizma djelovanja i razlika među serotipovima ključno je za njegovu sigurnu i učinkovitu primjenu. Temeljni učinak toksina proizlazi iz selektivne blokade oslobađanja acetilkolina, što dovodi do reverzibilne neuromuskularne i autonomne inhibicije te omogućuje terapijske koristi u nizu funkcionalnih i estetskih indikacija. Iako se nuspojave mogu javiti, najčešće su blage, prolazne i povezane s difuzijom toksina izvan ciljane regije, što čini stručnost aplikatora presudnim čimbenikom uspjeha. Uz odgovarajući odabir pripravka, pravilnu tehniku i dobro poznavanje anatomije, botulinum toksin ostaje siguran, predvidiv i izrazito vrijedan dodatak suvremenoj stomatološkoj praksi.
Popis literature:
- Benedetto AV. Botulinum toxins in clinical aesthetic practice. Volume One: Clinical Adaptations. 3rd ed. Boca Raton (FL): CRC Press/Taylor & Francis Group; 2018.
- Dong M, Stenmark P. The structure and classification of botulinum toxins.HandbExp Pharmacol. 2021;263:11-33. doi:10.1007/164_2019_342.
- Muñoz Lora VRM, Del Bel Cury AA, Jabbari B, Lacković Z. Botulinum toxin type A in dental medicine. J Dent Res. 2019;98(13):1450-1457. doi:10.1177/0022034519875053.
- Hong SO. Cosmetic treatment using botulinum toxin in the oral and maxillofacial area. Toxins. 2023;15(2):82. doi:10.3390/toxins15020082.
- Jankovic J. Botulinum toxin: state of the art. MovDisord. 2017;32(8):1131-1138. doi:10.1002/mds.27072.
- Jaspers GW,PijpeJ, Jansma J. The use of botulinum toxin type A in cosmetic facial procedures. Int J Oral Maxillofac Surg. 2011;40(2):127-133. doi:10.1016/j.ijom.2010.09.014.
- Flynn TC. Botulinum toxin: examining duration of effect in facial aesthetic applications. Am J Clin Dermatol. 2010;11(3):183-199. doi:10.2165/11530110-000000000-00000.
- DelpachitraSN, Sklavos AW, Dastaran M. Clinical uses of botulinum toxin A in smile aesthetic modification. Br Dent J. 2018;225(6):502-506. doi:10.1038/sj.bdj.2018.755.
- Miller J, Clarkson E. Botulinum toxin type A: review and its role in the dental office. Dent Clin North Am. 2016;60(2):509-521.doi:10.1016/j.cden.2015.11.007.
- Carruthers A, Kane MA, Flynn TC, et al. Botulinum toxin in clinical and cosmetic practice. Dermatol Surg. 2013;39(3 Pt 2):493-509. doi:10.1111/dsu.12147.
- Bentivoglio AR, Del Grande A, Petracca M, Ialongo T, Ricciardi L. Clinical differences between botulinum neurotoxin type A and B. Toxicon. 2015;107(Pt A):77-84.doi:10.1016/j.toxicon.2015.08.001.
- Jankovic J. Treatment of hyperkinetic movement disorders. Lancet Neurol. 2009;8(9):844-856. doi:10.1016/S1474-4422(09)70183-8.
- EleopraR, Rinaldo S, Montecucco C, Rossetto O, Devigili G. Clinical duration of action of different botulinum toxin types in humans. Toxicon. 2020;179:84-91. doi:10.1016/j.toxicon.2020.02.020.
- Kumar R, Singh BR. Botulinum toxin: a comprehensive review. Int J Mol Sci. 2025;26(2):777. doi:10.3390/ijms26020777.
- Swaminathan S. Molecular structures in clostridial neurotoxins. FEBS J.2011;278:4467-4485.
- Monash A, Tam J, Rosen O,SoreqH. Botulinum neurotoxins: history, mechanism, applications. J Neurochem. 2025;169(4):xxx-xxx.
- Rossetto O,PirazziniM, Fabris F, Montecucco C. Mechanism of action. Handb Exp Pharmacol. 2021;263:35-47.
- Pantano S,MontecuccoC. Blockade of neurotransmitter release. Cell Mol Life Sci. 2014;71:793-811.
- Martyn JAJ, Fagerlund MJ, Eriksson LI. Neuromuscular transmission.Anaesthesia. 2009;64 Suppl 1:1-9.
- Baskaran P, Günther R, Grafe K-M, et al. Acute and chronic effects ofBoNT-A. Br J Pharmacol.2014;171:1392-1405.
- Dressler D, Saberi FA. Mechanisms of action.EurNeurol. 2005;53:3-9.
- Keller JE. Recovery from poisoning. Neuroscience.2006;139:629-637.
- LaguenyA, Burbaud P. Botulinum toxin review. Neurophysiol Clin. 1996;26:216-226.
- Matak I, Lacković Z. Botulinum toxin A, brain and pain. ProgNeurobiol. 2014;119-120:39-59.
- BaguesA, Hu J, Alshanqiti I, Chung M-K. Analgesia mechanisms. Pharmacol Ther. 2024;259:108668.
- HosseindoostS, Askari Rad M, Inanloo SH, et al. Analgesic effects review. Mol Pain. 2024;20:17448069241275099.
- Zychowska M, Rojewska E, Makuch W, et al. Interleukins and analgesia.EurJ Pharmacol. 2016;791:377-388.
- Comtesse SM, Tavassoli F, Jabbari B. Update on dystonia and bruxism. Toxicon. 2025;108503.
- Yoshida K. Therapy for oromandibular dystonia. Toxins.2022;14:282.
- Majid OW. Botulinum toxins in OMFS. Int J OralMaxillofacSurg. 2010;39:197-207.
- Bakke M. Botulinum toxin intro. Toxins.2022;14:667.
- Moussa MS,BachourD, Komarova SV. Mandibular bone effects. J Oral Rehabil. 2024;51:404-415.
- Food and Drug Administration. BOTOX: FDA drug label. 2023 Nov 18.
- Serrera-Figallo MA, Ruiz-de-León-Hernández G, Torres-Lagares D, et al. Use in orofacial practice. Toxins.2020;12:112.
- Lim EC, Seet RC. Injection techniques. Acta Neurol Scand.2008;117:73-84.
- Pickett A. Dysport properties. Toxicon.2009;54:683-689.
- Dover JS, Monheit G, Greener M, Pickett A. Myths and realities. Dermatol Surg.2018;44:249-260.